Cadre général
Pour que des méthodes alternatives soient utilisées en substitution de tests sur animaux, il faut qu’elles aient été préalablement développées, reconnues par la communauté scientifique, validées.
En recherche fondamentale et appliquée, les méthodes substitutives sont utilisables librement, sans contrainte de standardisation. Ces méthodes sont scientifiquement reconnues par le processus classique de la validation par les pairs, i.e. la publication dans des revues scientifiques. Ce sont des outils pour la recherche voire même des objets d’étude. Utiliser le terme de « remplacement » est d’ailleurs en partie inapproprié car elles apportent une contribution originale et spécifique à des projets sans chercher à se substituer à des méthodes anciennes utilisant des animaux, qui deviennent éventuellement obsolètes.
Ces méthodes « reconnues » du point de vue scientifique peuvent être utilisées par les industriels en amont d’un processus de validation réglementaire pour du criblage par exemple, évitant des tests animaux et faisant gagner du temps sur le développement, en éliminant des molécules très toxiques ou sans efficacité.
Mais lorsqu’il s’agit de proposer un nouveau produit sur le marché, il est nécessaire de suivre un certain nombre d’étapes réglementaires, pour notamment garantir la sécurité du produit pour la santé humaine. Dans ce cadre, les alternatives aux tests animaux doivent suivre un parcours de validation afin de les standardiser et les inscrire dans la liste des protocoles autorisés.
Cette reconnaissance internationale est portée par l’Organisation de coopération et de développement économiques (OCDE), sous forme de lignes directrices, et/ou le Centre européen pour la validation des méthodes alternatives (ECVAM) au plan européen, pour les substances chimiques ; la Pharmacopée européenne pour les méthodes de contrôle de qualité des médicaments ; la normalisation CEN/ISO pour les milieux et les dispositifs médicaux.
Cette validation confère une garantie de qualité, un caractère opposable et une reconnaissance multilatérale.
Lorsqu’une équipe de recherche souhaite faire valider un test réglementaire sans animaux, le processus s’avère contraignant, long et coûteux, sans garantie in fine d’obtenir la validation du test. En effet, pour qu’une méthode alternative puisse être validée dans le cadre réglementaire, elle devra apporter, en plus de ce qui est demandé pour la reconnaissance scientifique (preuve de sa pertinence, de sa capacité à détecter les effets observés sur l’homme et l’animal), les preuves qu’elle est applicable de façon fiable et reproductible en dehors des laboratoires de recherche.
Le circuit de validation et acceptation réglementaire
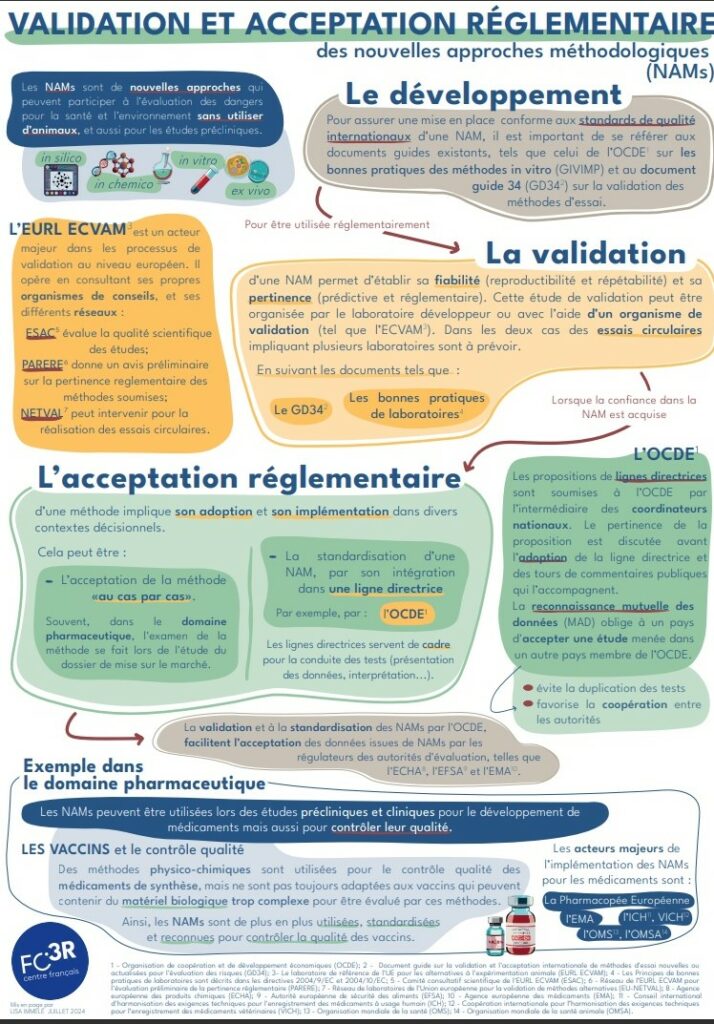
Infographie réalisée par le FC3R : téléchargeable ici




